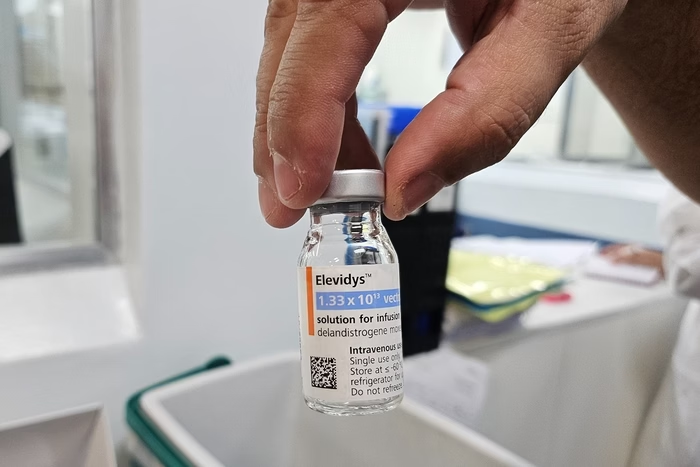
A Agência Nacional de Vigilância Sanitária (Anvisa) determinou a suspensão temporária do medicamento Elevidys, utilizado no tratamento da distrofia muscular de Duchenne (DMD).
A decisão foi motivada por suspeitas de que o remédio esteja relacionado a três mortes ocorridas nos Estados Unidos, incluindo dois adolescentes que recebiam o tratamento de forma experimental.
O remédio, que custa até R$ 17 milhões por dose, é considerado o mais caro disponível no Brasil. Ele começou a ser aplicado no Sistema Único de Saúde (SUS) em fevereiro deste ano e é indicado para crianças entre 4 e 7 anos que ainda conseguem se locomover sozinhas.
Nos EUA, os óbitos foram registrados em pacientes que já haviam perdido a capacidade de andar, um perfil que não se enquadra nas indicações da Anvisa no Brasil. Ainda assim, diante da gravidade dos relatos, a agência brasileira optou por interromper preventivamente o uso do produto até que a análise de risco esteja concluída.
Segundo a Anvisa, a medida visa preservar a segurança dos pacientes e revisar os protocolos de uso à luz das novas evidências internacionais. A agência também informou que a farmacêutica Roche, responsável pelo registro do Elevidys no Brasil, está colaborando com o processo.
A Roche afirmou que os tratamentos já agendados não serão suspensos e que a decisão sobre manter ou não a aplicação ficará a cargo dos médicos, em conjunto com as famílias. A empresa ressalta que, até o momento, não houve registro de efeitos adversos graves no perfil de pacientes no país.
A distrofia muscular de Duchenne é uma doença rara, hereditária e progressiva, que atinge especialmente os meninos. A condição causa a degeneração dos músculos e leva à perda gradual de funções motoras. O Elevidys atua por meio de terapia gênica e representa uma esperança para retardar os efeitos da doença.
Por Kátia Gomes | Daniela Gentil
VEJA TAMBÉM: Anvisa proíbe venda de medicamentos e suplementos alimentares; descubra quais